L’objectif du présent travail est de purifier les effluents liquides prétraités par les stations d’épurations (STEU) afin de les évacuer dans la mer ou autres milieux récepteurs. La technique utilisée est de bien oxygéner ces rejets liquides prétraités avant de les purifier par filtration percolation. Le filtrat récupéré est aussi soumis à une oxygénation profonde pendant un temps adéquat. Les absorbants que nous avons utilisés dans notre matrice filtrante sont le sable marin de taille granulométrique 100 µm, les cendres volantes et de l’argile. Le paramètre commun de ces adsorbats, d’après une analyse minéralogique effectuée par fluorescence X, est le taux élevé des silices et calcites qui sont des éléments très importants dans la rétention des métaux lourds. Les principaux paramètres analysés par ICP dans cette étude sont le Co, le Cr, le Cu, le Fe, le Pb, le Zn, le Co et l’As. Les résultats obtenus par ce système de traitement sont évalués à une réduction de 40?% pour le Cd, 70?% pour le Cr, 85?% pour le Cu, 95?% pour le Fe, 60?% pour le Pb et 99?% pour le Zn. Pour valider nos résultats, l’analyse par ICP des filtrats a été comparée avec celle de l’eau potable. Le filtrat obtenu par cette technique est parfaitement dans les normes d’utilisation pour des besoins industriels, comme liquide de refroidissement, ou en agriculture pour l’irrigation et l’arrosage des espaces verts.
INTRODUCTION
Les rejets liquides industriels sont très différents des eaux usées domestiques. Leurs caractéristiques varient d’une industrie à l’autre. En plus de matières organiques, azotées ou phosphorées, ces eaux peuvent également contenir des produits toxiques, des solvants, des métaux lourds, des micropolluants organiques, des hydrocarbures. Certaines d’entre elles doivent faire l’objet d’un prétraitement de la part des industriels avant d’être rejetées dans les réseaux de collecte.
Elles ne sont mêlées aux eaux domestiques que lorsqu’elles ne présentent plus de danger pour les réseaux de collecte et ne perturbent pas le fonctionnement des usines de dépollution. Avant d’être rejetées dans la nature, les eaux usées, c’est-à-dire les eaux déjà utilisées et dégradées par les usagers, doivent être traitées afin de ne pas altérer l’environnement. Ce processus est réalisé dans une station d’épuration des eaux usées (STEU). Lorsque l’eau usée arrive dans une station de traitement, elle va passer par une succession d’étapes visant à la purifier. On peut ainsi distinguer deux grandes phases.
Le prétraitement consiste à éliminer les corps les plus volumineux présents dans l’eau via le dégrillage. Dans cette même étape, on débarrasse également l’eau du sable qu’elle peut contenir (le dessablage), de ses corps gras (le déshuilage) et de la boue (la décantation primaire).
Le traitement secondaire est un traitement biologique, parfois couplé à des procédés physico-chimiques qui permettent une meilleure coagulation des boues et une meilleure fixation des phosphates en lien avec l’agriculture. Au cours de cette phase, de l’oxygène est injecté dans l’eau. Il y a, ensuite, la décantation secondaire, qui, elle, permet d’extraire, à nouveau, des matières boueuses contenues dans l’eau. C’est la clarification. L’apport principal de notre travail est de purifier les eaux prétraitées par les stations d’épurations par filtration percolation à travers notre matrice constituée de sable marin de taille granulométrique 100 µm, de cendres volantes issues de la combustion du charbon des centrales thermiques et d’argile.
Le filtrat ainsi récupéré est finalement soumis à une oxygénation profonde afin de le rendre conforme aux normes pour l’irrigation. Nous avons choisi ce genre de filtre naturel pour la simplicité de sa mise en œuvre, et surtout pour son efficacité et son rendement et terme de purification. Notre recherche a été axée principalement sur la réduction des métaux lourds dans ces rejets. Toutes nos analyses ont été effectuées par ICP (InductivelyCoupled-Plasma). Les métaux lourds que nous avons visés sont le cobalt, le zinc, le plomb, le fer, le cuivre, et le chrome, le cobalt et l’arsenic [1-10].
MATÉRIELS ET MÉTHODES



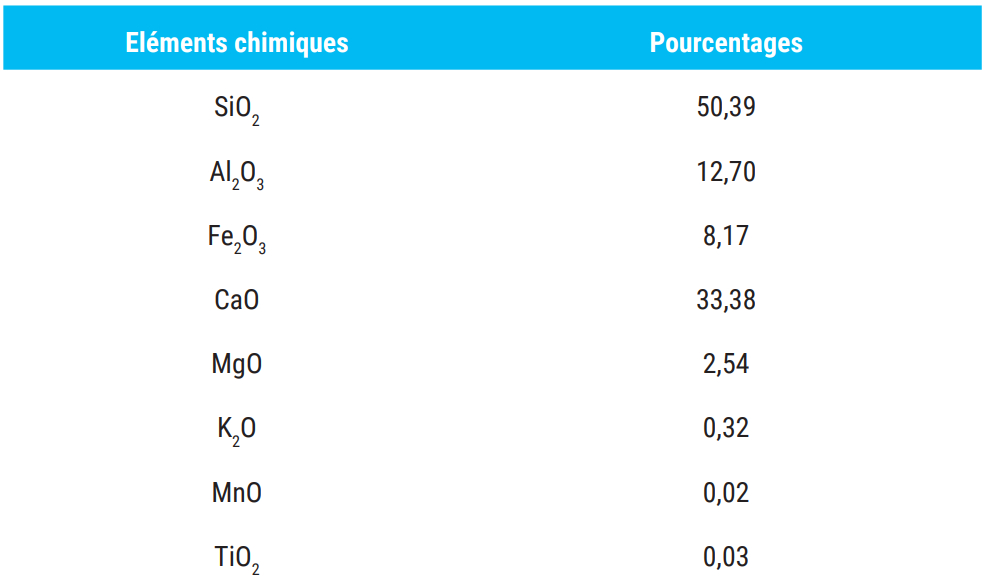
Le sable que nous avons utilisé dans nos expériences de filtration percolation a été prélevé le long du littoral de la ville d’El Jadida (figure 1). Ce dernier a été dans un premier temps soigneusement lavé et séché à 40°C dans une étuve, ensuite tamisé. Il a été finalement analysé par fluorescence X pour avoir une idée très précise sur le taux de calcite et de silice. L’analyse chimique avait pour but d’indiquer précisément les caractéristiques chimiques du sable naturel utilisé dans nos expériences. Le résultat, résumé dans le tableau 1, montre que le sable de taille granulométrique 100 µm contient une grande quantité d’alumine et est très concentré en silice ce qui favorise l’interaction avec les oxydes contenus dans les cendres pour une bonne absorption [11-13]. Les cendres volantes sont les plus courants parmi les déchets de charbon utilisés comme adsorbants, et dans cette étude, les cendres ont été extraites de la centrale thermique de Jorf Lasfar «JLEC», située à 17 km de la ville d’El Jadida.
Les cendres volantes (Figure 2) sont produites par les précipitâts dans les cheminées de la centrale électrique au charbon. Elles apparaissent comme des particules sphériques, d’une couleur grise typique. Les cendres volantes sont bien connues pour leurs propriétés pouzzolaniques et leur surface chargée négativement. Pour améliorer la compréhension du processus de filtration, les échantillons de cendres ont été soumis à la fluorescence X pour indiquer leur composition chimique, puis au tamisage granulométrique pour évaluer la distribution des tailles de grains. La structure cristalline et la surface de chaque type de cendres ont été étudiées par Taoufiq et al, qui a examiné les cendres extraites de la même centrale électrique «JLEC».
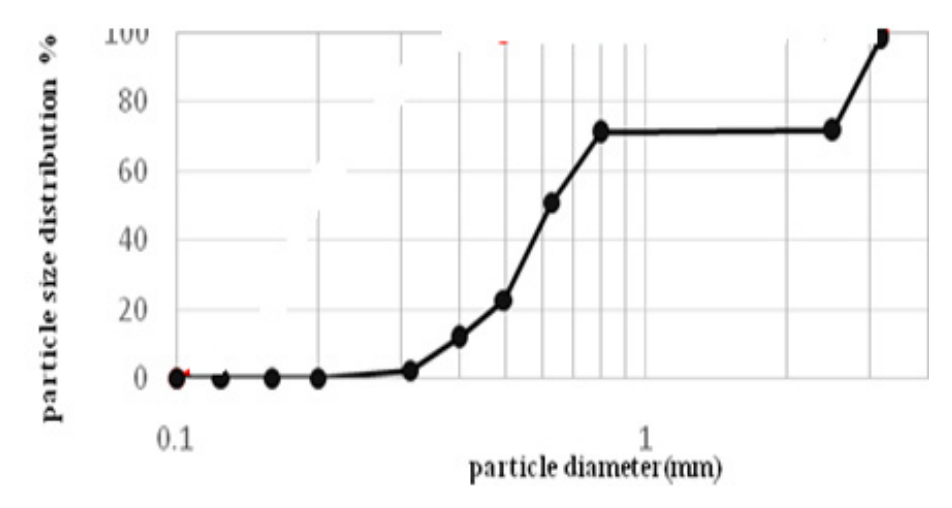
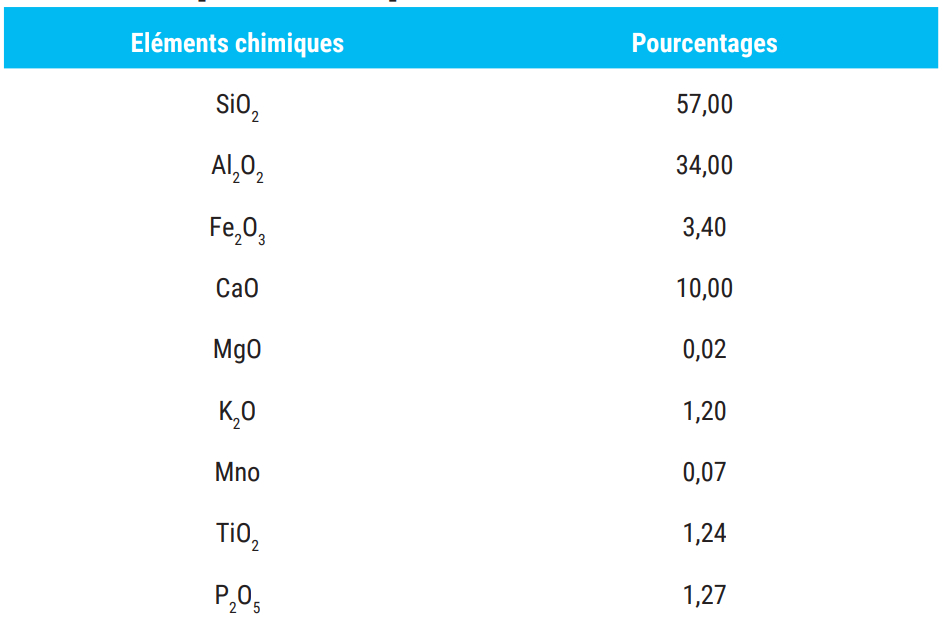
Leurs résultats seront pris en considération lors de la discussion d’adsorption puisque nous utilisons la même source de cendres [14]. La composition chimique des cendres volantes analysée par fluorescence X est donnée dans le tableau 2 ci-dessous. La distribution granulométrique des cendres volantes est schématisée dans la figure 3. La photo ci-dessous illustre la structure morphologique des cendres obtenue par microscope à balayage électronique MEB avant filtration: elles se présentent sous la forme de particules poreuses de tailles irrégulières. Cela va dans le sens signalé par Wei-ling Sun et al, qui ont étudié une cendre de provenance similaire. Ils ont montré que la plupart des grains de cendre se présentent sous forme de sphères creuses ou de sphères comblées par des sphères plus petites [15-16].
Les échantillons d’argiles (figure 4) ont été recueillis dans les environs d’El Jadida précisément dans la région de Sebt Oulad Bouaziz. C’est de l’argile blanche (Kaolinite) connu par sa couleur qui provient essentiellement du pourcentage élevé d’alumine (environ 23%). Elles sont caractérisées par leur charge négative.
Le kaolin, friable et réfractaire est composé principalement de kaolinite, soit des silicates d’aluminium avec un peu de quartz libre et certains minéraux d’argile et de feldspath, ayant une surface spécifique importante et une grande capacité d’adsorption et de rétention de différents polluants organiques et minérales. Des travaux récents ont étudié la faisabilité de l’utilisation de différentes argiles minérales et synthétiques telles que la kaolinite et la montmorillonite et ont démontré leur efficacité pour l’élimination des métaux lourds et différents polluants toxiques des eaux usées.

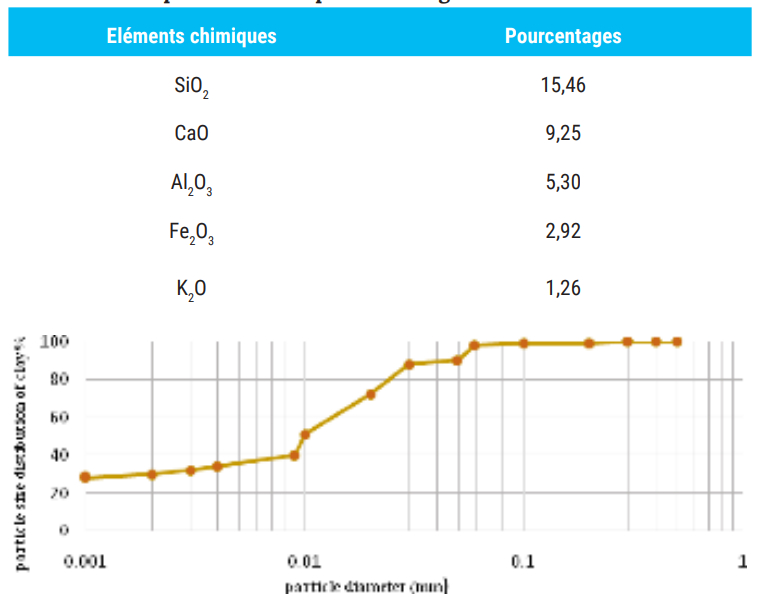
La distribution granulométrique de l’argile que nous avons utilisée est donnée la figure 5 ci-dessous [17-18]: Sa composition chimique après analyse par la technique de la fluorescence X est donnée dans le tableau 3 et le spectre obtenu par diffraction des rayons X est schématisé dans la figure 6. Le résultat montre que l’argile utilisé dans nos expériences contient comme éléments majeurs de la silice, de l’alumine et du fer, qui augmente l’interaction avec les oxydes contenus dans les cendres de charbon.
Les effluents liquides prétraités ont été collectés auprès de la station d’épuration d’El Jadida. Nous avons dans un premier temps, bien oxygéné nos effluents liquides prétraités pendant 30 min, puis effectué nos expériences de filtration percolation à travers notre matrice purifiante, formée de sable marin de taille granulométrique 100 µm, de cendres volantes et d’argile blanche.
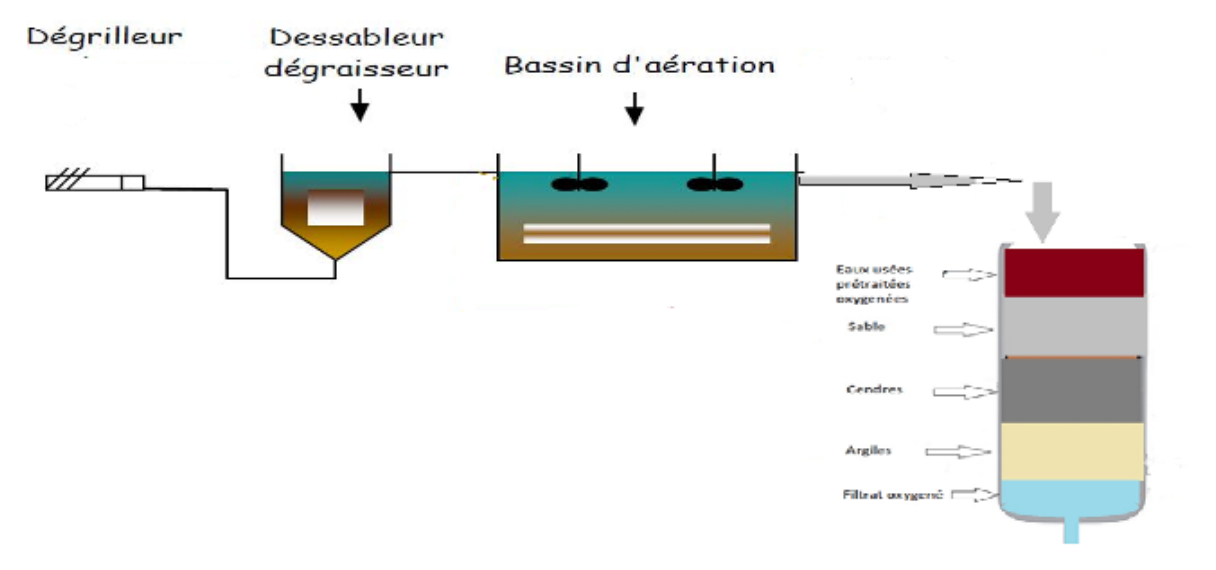
Le montage expérimental que nous avons utilisé est schématisé sur la figure 7, il s’agit d’une colonne verticale, de 20 cm diamètre, et de 80 cm de hauteur. L’alimentation du système se fait exclusivement par des eaux prétraitées et oxygénées et l’écoulement se fait en percolation à travers le substrat.
Le filtrat récupéré a été aussi bien oxygéné afin de se conformer aux normes internationales avant toute évacuation dans la mer, les lacs ou autres milieux récepteurs. Ce rejet est transparent et inodore.
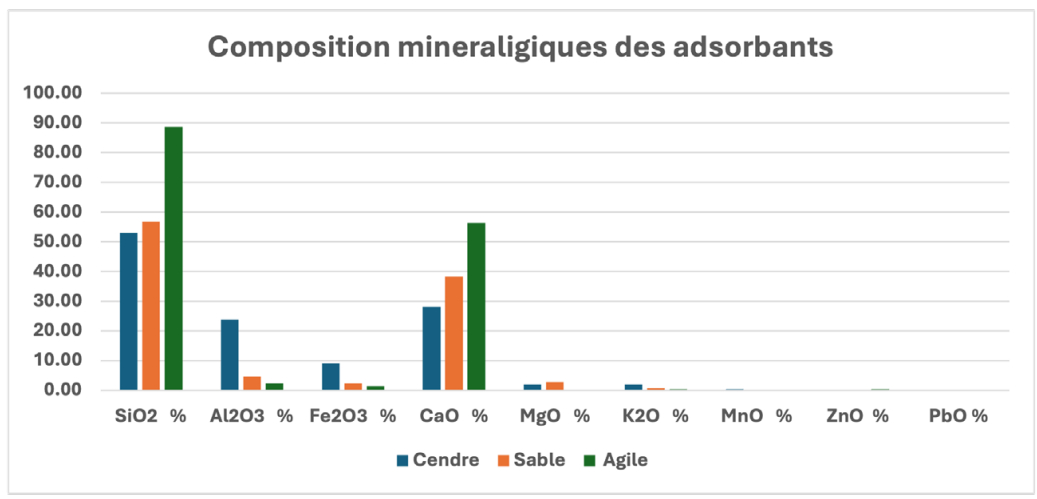
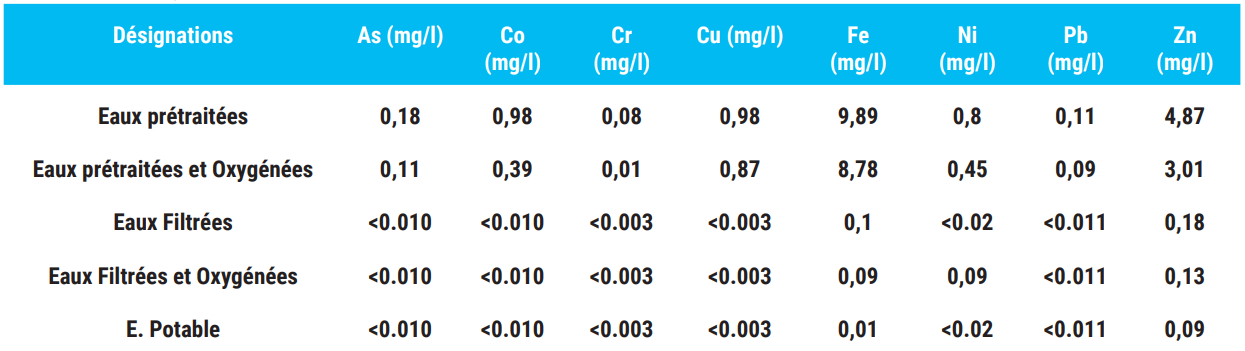
L’histogramme ci-dessous (figure 8), montre que les trois adsorbants formant notre matrice sont riches en silice et en calcite, ce qui est très intéressant car ces dernières sont très importantes dans la rétention des métaux lourds éventuellement présents dans nos effluents avant et après filtration. Le tableau 4, présente en ppm le taux de quelques éléments, détectés dans les effluents étudiés dans leurs état prétraité, puis oxygénés avant filtration percolation, et enfin oxygénées avant et après filtration percolation. Pour mieux comprendre et constater les abattements obtenus après filtration, nous avons présenté nos résultats sous formes d’histogrammes.
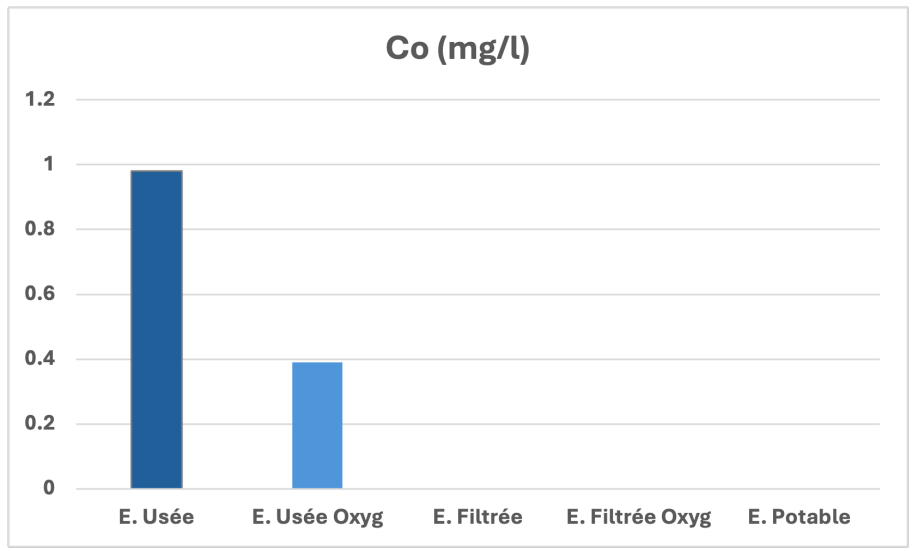
Evolution du cobalt
Le cobalt dans les eaux usées provient principalement de la coloration des verres, de la céramique et de l’émail au moyen de dérivés du cobalt. Dans l’industrie chimique, le cobalt intervient dans les catalyseurs homogènes et hétérogènes pour la synthèse des carburants, des alcools et des aldéhydes. La filtration à travers nos adsorbants a éliminé considérablement la concentration du cobalt. Cet abattement très important est expliqué par l’immobilisation au niveau du substrat via des mécanismes tels que l’adsorption au niveau des sites d’échanges, la fixation à la matière organique, l’incorporation dans la structure de l’argile et la précipitation sous forme de composés insolubles (figure 9) [20-22].
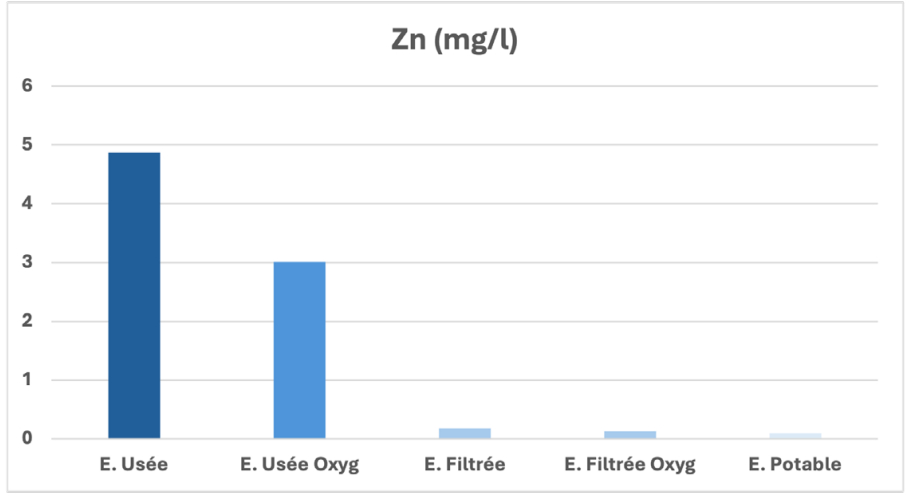
Evolution du zinc
La concentration du zinc dans les eaux usées prétraitées a pour origine l’exploitation minière, la combustion du charbon, des déchets, et l’industrie de l’acier. Le zinc, relativement mobile est facilement adsorbé par les constituants du sol organiques et minéraux. Le zinc peut donc être mobile et migrer facilement en profondeur. Le résultat obtenu après oxygénation et filtration par notre matrice est très intéressant car les abattements de ce métal ont atteint presque 95%. (Figure 10) [23-25].
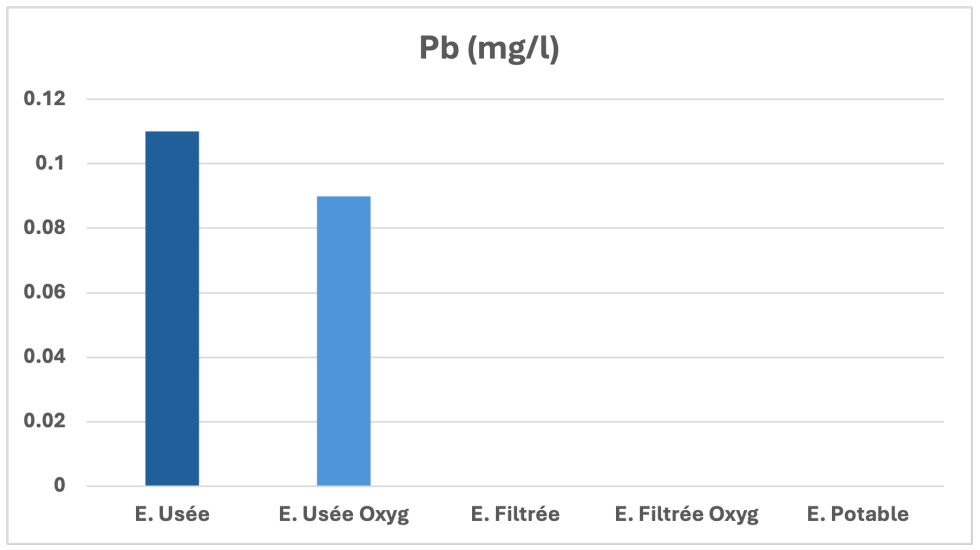
Evolution du plomb
La purification des rejets liquides par les différents adsorbants a permis une réduction de 99% de ce dernier (figure 11). L’élimination presque totale du Plomb s’explique par les différents minéraux argileux présents dans l’argile utilisée, particulièrement la palygorskite [26-27].
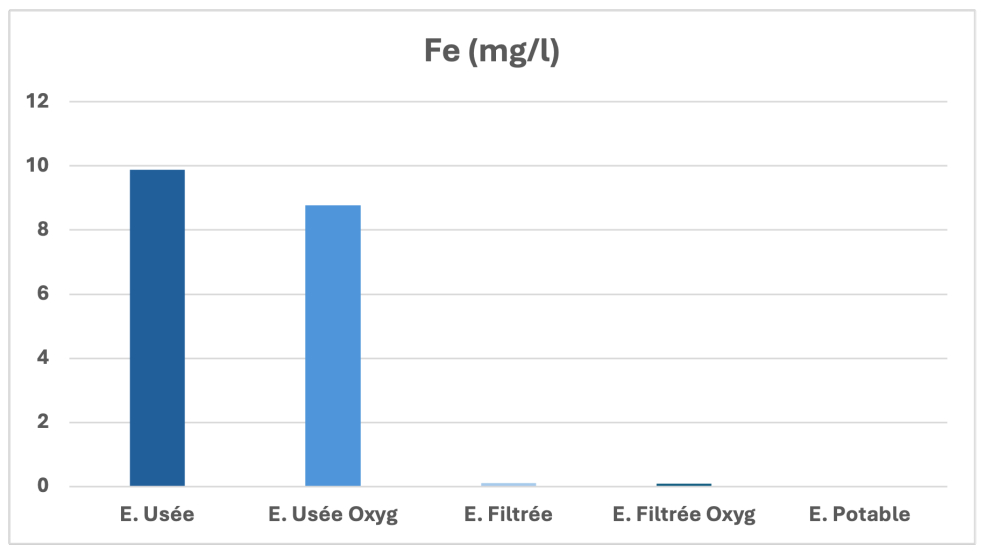
Evolution du fer
Le fer est l’un des métaux les plus abondants de la croûte terrestre. Il est présent dans l’eau sous trois formes, le fer ferreux Fe2+, le fer ferrique Fe3+ et le fer complexé à des matières organiques (acides humiques, fulviques, tanniques,…). Son origine au niveau industriel peut s’expliquer par l’exploitation minière, la sidérurgie, la corrosion des métaux. Le fer donne aussi un goût métallique à l’eau rendant désagréable sa consommation. La filtration des eaux prétraitées par la STEP, par oxygénation à la fois des eaux prétraitées et du filtrat à travers nos adsorbants a permis une réduction totale de cet élément de 98% (figure 12). Cette élimination est due à des micro-organismes présents dans l’argile, les cendres volantes et le sable [28].
Evolution du cuivre
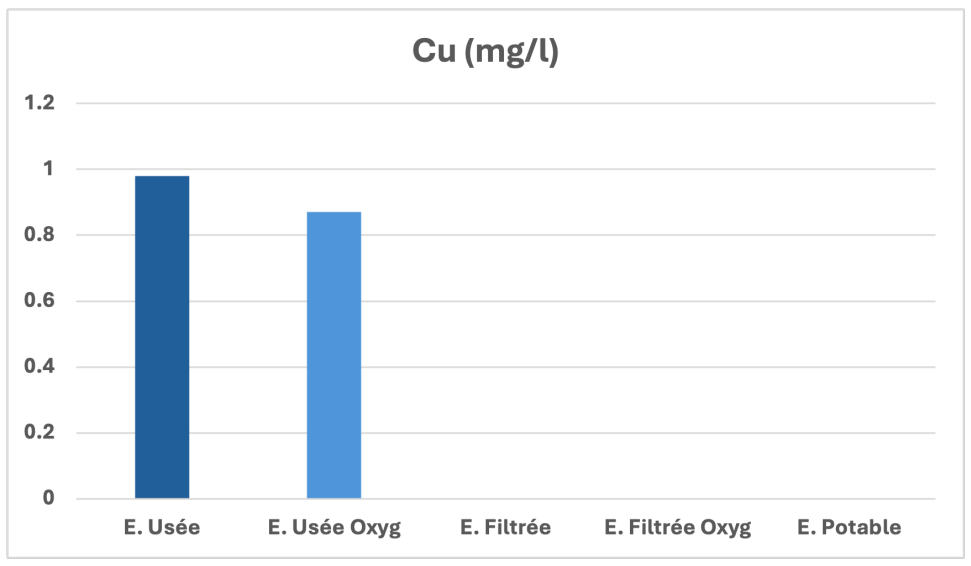
La présence de cuivre dans l’eau est surtout attribuable au relargage des composants des réseaux de distribution et des systèmes de plomberie qui renferment du cuivre. Le cuivre a été, et continue d’être, largement utilisé dans des applications liées à l’eau potable, notamment dans les tuyaux de plomberie résidentielle et les raccords. La présence de cuivre dans l’eau peut altérer le goût de celle-ci et tacher le linge et les accessoires de plomberie, même lorsque les concentrations sont inférieures à la norme internationale proposée.
Bien que ces concentrations ne soient associées à aucun effet nocif, elles peuvent avoir une influence sur l’acceptabilité de l’eau par les consommateurs et nuire à d’autres priorités relatives à la qualité de l’eau, comme la limitation du plomb. L’oxygénation des eaux prétraitées par la station d’épuration, avant filtration à travers notre matrice , ainsi que la soumission du filtrat obtenu à une oxygénation supplémentaire ont permis une réduction de ce métal de 99% (figure 13) [29].
Evolution du chrome
Le chrome est un élément métallique sans goût et sans odeur naturellement présent dans les pierres, la terre et les plantes. Il existe deux formes plus communes de chrome naturel. Le chrome trivalent, essentiel à notre alimentation, est présent dans les fruits, les légumes, les viandes, la levure et les graines Le chrome hexavalent, naturellement présent dans l'environnement, est une conséquence de l’érosion. Il peut aussi provenir de processus industriels et se retrouver dans l'environnement du fait d’un mauvais entreposage, de déversements ou d’une mauvaise mise au rebut des déchets industriels.
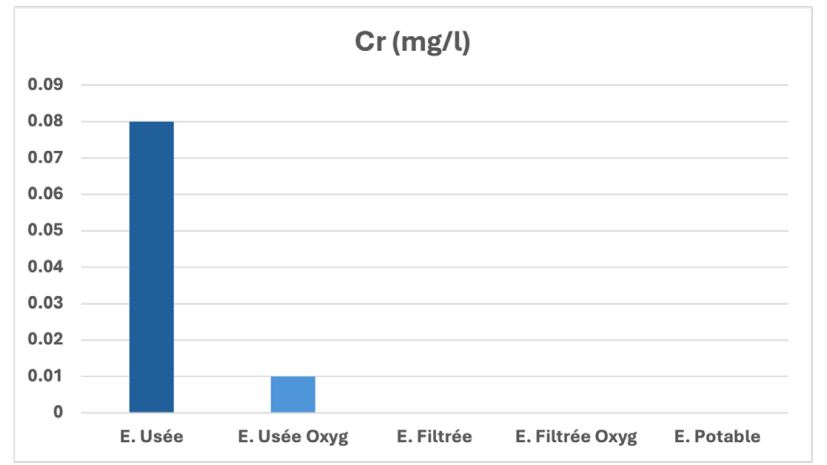
Ces deux formes de chrome sont utilisées dans l’industrie pour le chromage, la teinture et la pigmentation, le tannage du cuir et la conservation du bois. Les personnes qui travaillent avec le chrome dans l’industrie ou qui vivent à proximité d’un site d’enfouissement de déchets dangereux sont les plus à risque d’être exposées au chrome. Selon les réglementations sur l’eau potable de l’Environnemental Protection Agency ou EPA (Agence pour la protection de l’environnement), la limite de sécurité du chrome dans l’eau est de 100 parties par milliard (ppm). Notre technique de filtration nous a permis d’eliminer de presque 99% cet élément (figure 14) [30-32].
Evolution du nickel
Il existe des sources naturelles de nickel mais il est principalement obtenu à partir de minerais de nickel sulfurés (pyrrhotite, nickeliferreuse, pentlandite, chalcopyrite) dans lesquels sont également présents le fer et le cuivre. Les sources d’émission vers les eaux superficielles sont les rejets diffus agricoles, du fait de la présence naturelle de Nickel dans les sols, et aussi de la présence artificielle en provenance d’engrais phosphatés. On peut noter la difficulté et/ou impossibilité de supprimer le nickel dans certaines applications particulières (alliages, aciers inoxydables,); ainsi qu’une durée de vie importante des produits contenant du nickel.
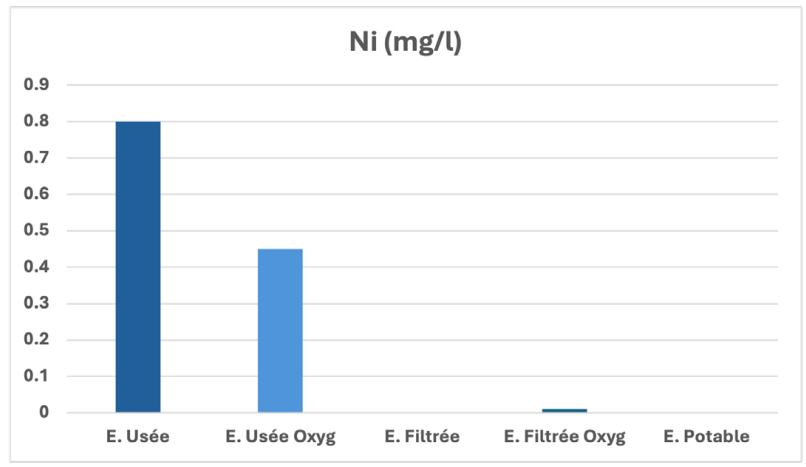
De plus, on assiste au recours à des produits contenant du nickel en remplacement des produits présentant un fort impact pour l’environnement (remplacement des batteries aux plomb, cadmium, … par des batteries NiMH). L’usage de produits contenant du nickel dans une optique de préservation de l’environnement (du nickel est utilisé pour les batteries des véhicules électriques et hybrides, …) est encouragé. Ainsi, on observe la croissance du marché de l’ensemble des produits contenant du nickel et la présence d’apports industriels diffus à l’échelle du territoire. On constate d’après la figure 15, une élimination presque totale de cet élément ce qui conforte la validité de notre technique expérimentale [33-35].
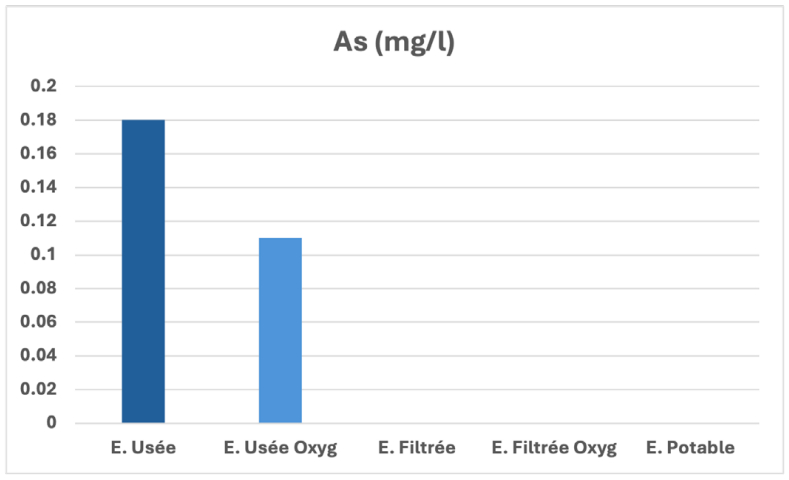
Evolution de l’arsenic
Toute matière vivante contient des traces d’arsenic. Les aliments sont la principale source d’exposition à l’arsenic, suivis de l’eau potable, du sol et de l’air. L’eau potable représente la principale source d’exposition uniquement chez les personnes vivant près d’une source d’arsenic. L’arsenic s’infiltre naturellement dans les lacs, les rivières ou l’eau souterraine lorsque des dépôts minéraux ou des roches qui en contiennent se dissolvent. L’arsenic peut aussi s’infiltrer dans l’eau lors du déversement de déchets industriels ou lorsque des particules se mêlent à la poussière ou sont dissoutes dans la pluie ou la neige.
Ces particules peuvent être rejetées dans l’environnement par : la combustion de combustibles fossiles (notamment le charbon); par la production de métaux (extraction d’or et de métaux communs, par exemple); les activités agricoles (utilisation de pesticides et d’additifs pour l’alimentation animale); ou par l’incinération de déchets. L’oxygénation des eaux récupérées après filtration percolation à travers nos adsorbants a permis aussi une élimination quasi-totale de cet élément toxique (figure 16) [36-39]. Les pourcentages moyens des abattements des différents éléments toxiques étudiés dans ce travail sont rassemblés sur le tableau 5 ci-dessous :

CONCLUSION
Le traitement des eaux issues des stations d’épurations (STEU) par oxygène que ce soit avant ou après filtration à travers les adsorbants utilisés à savoir le sable marin, les cendres volantes et l’argile, peut être utilisé dans deux optiques différentes. Tout d’abord l’oxygène peut être introduit dans l’eau en tant que traitement lui-même, car un taux d’oxygène optimal dissous dans l’eau permet d’équilibrer les pics de DCO / DBO (Demande Chimique en Oxygène / Demande Biochimique en Oxygène), c’est-àdire la «respiration» des micro-organismes présents dans l’eau. Ce traitement permet de contrôler la prolifération de ces micro-organismes et de favoriser la dégradation matières organiques par ces micro-organismes.
Le traitement de l’eau par oxygénation est principalement utilisé dans les stations d’épuration des eaux usées. La seconde optique de l’oxygénation de l’eau intervient lors de la production d’eau potable: l’eau, pour être consommable, doit contenir une certaine proportion d’oxygène qu’il convient de réguler. L’atout majeur du traitement de l’eau par l’oxygène réside dans le fait qu’il n’utilise aucun élément polluant, l’oxygène étant présent naturellement dans notre environnement. L’oxygénation des eaux usées est un processus servant à l’aération, la purification et au traitement de l’eau. Cette dernière suite à ce traitement est recyclée ou réutilisée dans le milieu naturel.
Elle peut aussi plus tard être transformée en eau potable. Ce processus s’effectue grâce à une introduction d’oxygène dans l’eau en guise de traitement (donc son aération). Cette opération a pour but d’ajuster la demande chimique en oxygène de cette dernière. L’aération et l’apport d’oxygène dans l’eau contribuent aussi à augmenter la prolifération des bactéries et des micro-organismes. Ce type de traitement s’effectue généralement dans les stations d’épuration. Par ailleurs, l’oxygénation peut aussi servir dans le cadre de la production d’eaux potables. De même la filtration par le sable marin ajoutée à la matrice formée par les cendres volantes, et l’argile blanc nous a permis d’identifier les points suivants:
• La richesse en silice de l’ensemble des adsorbants utilisés permet une réduction plus importante des métaux lourds étudiés dans ce travail.
• La réaction pouzzolanique entre les cendres volantes et la chaux du sable permet la stabilisation des métaux lourds avec des valeurs inferieures aux normes marocaines de rejets directs.
• Les eaux filtrées récupérées sont parfaitement dans les normes pour une réutilisation dans l’irrigation et l’arrosage des espaces verts.


