La formation de biofilms sur les surfaces des canalisations d’eau potable constitue un risque important pour le consommateur. Nous avons réussi, à l’aide d’une nouvelle formule intégrant des huiles naturelles du Maroc, à élaborer des tubes dotés de propriétés mécaniques satisfaisantes. Un test d’adhésion a été conduit, les observations en MEB confirment l’effet anti-adhésion. La spectroscopie infrarouge et l’analyse statistique prouvent des modifications structurales des groupements exposés en surface des canalisations. L’angle de contact permet la détection d’éventuelles modifications de l’hydrophobicité et du caractère acido-basique, ce qui peut expliquer certaines variabilités observées après test d’adhésion.
Les biofilms sont des dépôts qui se forment naturellement et spontanément dans les réseaux de distribution d’eau potable. Parfois spectaculaires, ils sont le plus souvent inoffensifs. Ils doivent cependant être maitrisés, car ils peuvent abriter des germes pathogènes, qui, suite à un détachement, peut fortement dégrader la qualité microbiologique de l’eau au cours de son transport dans les réseaux de distribution. Pour lutter contre ces nuisances, une stratégie préventive, qui consiste à réagir aux stades précoces de leur formation, s’avère pertinente. Les mesures curatives, telles que la réhabilitation de réseaux, semblent être en effet très coûteuses [1-4].
Historiquement, de nombreux matériaux ont été utilisés dans les canalisations pour transporter l’eau de l’usine de production vers le consommateur. Mais ceux-ci sont de plus en plus souvent remplacés aujourd’hui par des canalisations en plastique. Ces derniers, n’ayant cessé de gagner en popularité, ils sont devenus aujourd’hui les matériaux de prédilection dans de nombreux pays [1-4].
Au cours de cette étude, nous nous sommes intéressés plus spécialement aux canalisations en poly chlorure de vinyle PVC. L’objectif est orienté vers la conception de matériaux de canalisation anti-adhésion en modifiant la formulation du tube généré par le procédé d’extrusion. Sachant que les résines de PVC ne sont jamais utilisées seules car leur stabilité thermique à la température de transformation est trop faible. Il est courant qu’on leur adjoigne des additifs. Comme la plupart des polymères, le PVC a tendance à coller et à se dégrader sur le métal chaud des machines de transformation. Parmi les additifs utilisés, figurent les lubrifiants et les stabilisants [5]. Nous nous sommes orientés vers la composante de lubrification, étant donné le lien étroit avec le phénomène du collage et d’adhésion et le fait qu’au niveau de la formule du tube, cette dernière migre naturellement vers la surface. Le fait d’utiliser une huile biologiquement active pourrait inhiber la formation de biofilms bactériens au niveau de la surface des canalisations.
Il a été rapporté que l’huile de cade (Junipers oxycedrus) et d’ail (Allium sativum), possèdent des propriétés antibiotiques ainsi que des propriétés antifongiques et antibactériennes [6-11]. Par ailleurs, l’huile de ricin (Ricinus communis) est connue pour ses propriétés physiques uniformes et stables dans le temps, c’est pourquoi elle est couramment utilisée comme standard absolu pour les mesures de viscosité. La présence de groupements hydroxyles polaires permet à cette huile d’être directement compatible avec une grande variété de résines naturelles et synthétiques, de cires, de polymères et d’élastomères pour lesquels elle peut même servir de plastifiant, émollient et de lubrifiant, ainsi que de remarquables propriétés de mouillage et de dispersion de colorants, pigments et fillers [12]. Cette huile est également connue pour être riche en ricinoléine, glycéride de l’acide ricinoléique, qui lui confère des propriétés purgatives, ainsi qu’un pouvoir lubrifiant [12-13].
Dans cette étude, la proportion qui concerne le lubrifiant dans la formulation des tubes PVC sera partiellement remplacée par trois huiles naturelles abondantes : l’huile de cade, d’ail et de ricin (à raison de 10 % dans la proportion concernant le lubrifiant).
Matériel et méthodes
Formulation et élaboration du tube PVC
.jpg)
Les canalisations testées ont été fabriquées par extrusion. Environ 100 kg de différents composants (tableau 1) ont été mélangées dans un turbo-mélangeur pendant 5 minutes à 160 °C, puis malaxés jusqu’à homogénéisation et refroidis jusqu’à environ 40 °C, avant d’être envoyés vers l’extrudeuse à un débit de 100 kg/heure. La température de l’extrudeuse varie de 175 °C à l’entrée, 185 °C au milieu et 165 °C à la sortie de la filière. Le tube sort en continu et est refroidi avant d’être coupé à la longueur voulue. Le tableau 1 montre les différentes formulations ainsi utilisées.
Les huiles utilisées sont des huiles commerciales : l’huile de cade se présente sous forme d’un liquide limpide, homogène et noir à reflet rougeâtre, obtenue par carbonisation (pyrolyse) du tronc et des grosses branches des vieux cardiers du moyen Atlas du Maroc, selon un procédé connu sous le nom de per ascensum. L’huile de ricin et d’ail sont obtenues par un procédé d’extraction conventionnelle des huiles, initialement par broyage à l’aide d’une presse à vis sans fin, afin d’en extraire l’huile de première pression qui subit souvent une filtration ultérieure [6-13].
Modèles biologiques
Les souches bactériennes Pseudomonas aeruginosa ATCC27853 et Escherichia coli ATCC25922 sont utilisées en tant que modèles biologiques pour réaliser les tests d’adhésion. Ce sont des bacilles gram négatif couramment utilisés pour le contrôle qualité des eaux et l’efficacité du protocole de la désinfection d’eau potable [1].
.jpg)
Préparation de la suspension bactérienne
Pour chaque culture bactérienne, une pré-culture a été préparée par ensemencement des bactéries suivi d’une incubation durant une nuit à 37 °C dans le milieu Luria Bertani liquide (LBL). Puisqu’il est toujours intéressant d’exécuter les tests avec des bactéries dans leur phase exponentielle de croissance, une seconde culture est ensuite préparée à partir de cette première culture en ajoutant du milieu de culture LBL stérile dans un rapport 1/1, (v/v), cette dernière étant incubée 90 minutes à 37 °C. Les cellules bactériennes sont ensuite récupérées par centrifugation à 8.400 g pendant 15 min, et lavées deux fois avec de l’eau potable minérale stérile et finalement diluée avec cette même eau jusqu’à obtenir une suspension bactérienne de densité, optique à 405 nm, comprise entre 0,7 et 0,8.
Préparation des supports d’adhésion
À partir des tube PVC ainsi produits, on découpe des surfaces de 0,25 cm² qui seront nettoyées et désinfectées pour éliminer les impuretés minérales et organiques de la surface [1-3].
Test d’adhésion
Les tests d’adhésion consistent à mettre en contact horizontal les supports avec la suspension bactérienne dans un milieu constitué d’eau potable. Le contact dure environ 120 min. Ensuite, la suspension bactérienne est éliminée, la surface est secouée doucement par l’eau potable stérile afin d’éliminer toutes les bactéries qui n’ont pas adhéré et qui sont susceptibles de fausser les mesures de densité cellulaire adhérée. Chaque surface est examinée par observation (moyenne de 3 dénombrements) en MEB (Philips, Modèle XL30) après la phase classique de la préparation de l’échantillon y relative.
Tests et essais mécaniques
Les tests ont été réalisés conformément à la norme ISO 6042 : 2002 [19]. La machine d’essais mécaniques de compression est une machine électromécanique de type 3R modèle RP 25 ATF (Recherche & Réalisations Rémy, France).
Analyse infrarouge
Des analyses spectrales dans le moyen infrarouge (MIR, entre 4.000 cm-1 à 400 cm-1, 2,5 μm à 25 μm) en mode ATR ont été réalisées sur des petits morceaux de canalisations par un spectrophotomètre (Thermo Scientific-Nicolet 6700). L’analyse en composante principale (ACP) a été utilisée pour comparer les spectres collectés. Cette méthode permet, en réduisant fortement la dimensionnalité de données souvent redondantes, d’obtenir une carte factorielle permettant d’évaluer les ressemblances d’après les distances euclidiennes séparant les individus (spectres) ou groupes d’individus (clusters). Cette analyse a été effectuée à l’aide du logiciel Statistica®.
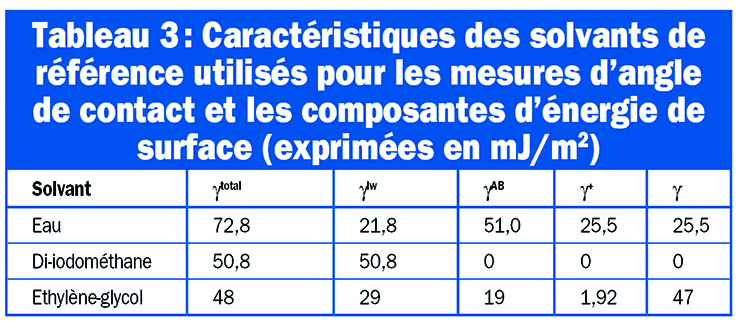
Angle de contact
L’eau (W), l’éthylèneglycol (EG) et le di-iodométhane (DM) ont été utilisés comme solvants de référence pour la caractérisation physico-chimique par l’angle de contact, le tableau 3 présente les composantes énergétiques de surface de chacun d’entre eux [15-18].
Une goutte de 2 µl est formée à l’extrémité d’une seringue pour être déposée automatiquement sur la surface de l’échantillon à tester. Une image numérique est aussitôt acquise à l’aide d’une caméra CCD disposée sur un goniomètre (Visiodrop-MCAT de GBX SC Instruments, France). Trois mesures sont effectuées pour chaque échantillon. De la valeur moyenne calculée, les énergies libres de surface sont déterminées : totale, dispersive et acide-base [1-3, 15-16].
Résultats et interprétations
Propriétés mécaniques du tube
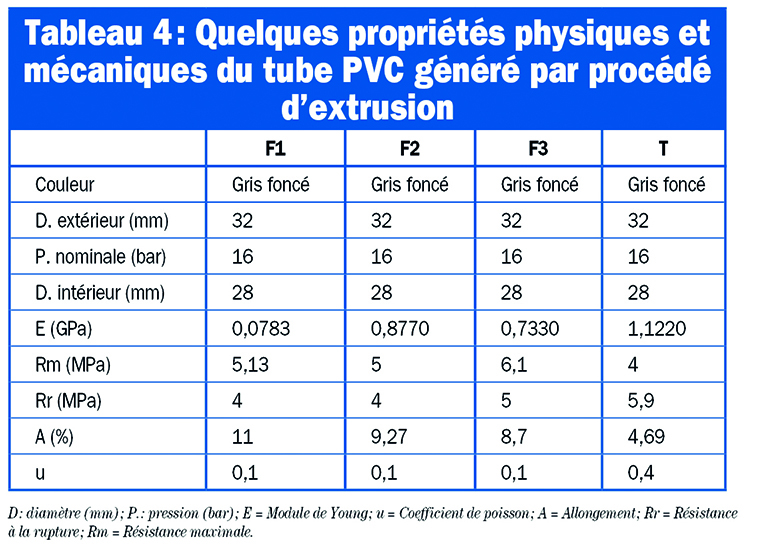
Le tableau 4 présente les résultats des tests mécaniques ainsi conduits.
Sous sa forme pure, le PVC est un matériau d’une rigidité meilleure dans la famille des polymères. Cependant, il devient fragile à faible température. Son module de Young, caractérisant sa rigidité se situe entre 0,35 et 2,5 GPa [20]. D’après le tableau, on remarque que T présente la plus grande rigidité de par son module de Young qui est relativement élevé. Il est suivi de F3, F2 et enfin F1. Le coefficient de Poisson renforce la remarque observée. En effet, le coefficient de Poisson de T est le plus grand, sachant que le maximum de ce coefficient est 0,5.
Analyse spectrale par infrarouge
.jpg)
La figure 1 présente les spectres infrarouges collectés pour les morceaux de canalisations testés (A) et les spectres déduits par dérivation pour pré-visualiser les zones de variabilités (B).
.jpg)
Les figures 2 et 3 présentent une analyse en composante principale dans le domaine spectral étudié. La figure 2 est la carte ACP qui représente la projection des spectres dans le plan factoriel constitué par CP1 (58,32 %) et CP2 (25,75 %). La figure 3 est la carte ACP qui indique la projection des spectres dans le plan factoriel constitué par CP1 (58,32 %) et CP3 (15,93 %).
.jpg)
D’après la figure 2, on observe que le spectre F1 est distingué des spectres concernant F2, F3 et T de par CP1. Pour identifier les nombres d’ondes corrélés avec cet axe, la corrélation entre ces derniers et les composantes principales a été déterminée. Les résultats sont présentés dans la figure 4.
La figure 4 présente la corrélation entre les nombres d’ondes et les trois premières composantes principales dans le domaine spectral étudié.
.jpg)
D’après la figure 4, on remarque qu’une forte corrélation avec les composantes principales CP1 et CP2 est fortement enregistrée vers : 1.140 et 1.200 cm-1 : zone qui concerne la vibration de la liaison C = S de composante de l’huile d’ail (figure 5).
.jpg)
La zone entre 1.200 et 1.350 cm-1 : zone qui pour le cade et le ricin manifeste plusieurs modes de vibrations confirmés par leurs aspects larges, à savoir : ph-O-C élongation de composantes dans l’huile de cade (figure 7), C-O élongation des esters du ricin et OH déformation dans le plan de la liaison alcool secondaire de composantes du ricin (figure 7).
.jpg)
Les plus fortes corrélations avec CP3, sont enregistrées dans la zone entre 2.800 et 3.050 cm-1. Cette zone permet, selon le biplot enregistré dans la figure 3, de séparer le spectre relatif à F3 de ceux relatifs à F1 et F2, en effet, le ricin est connu par sa richesse en récinoléines, acide ricinoléique, les groupements acides carboxyliques qui les composent peuvent manifester une vibration forte et très large dans cette zone associée au mode O-H élongation (figure 7).
.jpg)
Angle de contact
Il est généralement admis que les interactions non-spécifiques jouent un rôle important dans l’adhésion initiale de bactéries planctoniques sur un support. Les forces mises en jeu impliquent des interactions de Lifshitz-van der Waals (LW), électrostatiques (EL) et acide base (AB) [1]. Utilisant l’approche acide-base, établie par van Oss et al. [16], et qui constitue l’approche DLVO étendue (XDLVO) pour la mesure des interactions LW et AB, les composantes de la tension de surface acides, basiques et dispersives peuvent être déterminées à partir de la mesure d’angles de contact en utilisant trois solvants de références [1, 16]. Les résultats de mesure d’angle de contact et de caractérisation énergétique des différentes surfaces élaborées sont résumés dans le tableau 5.
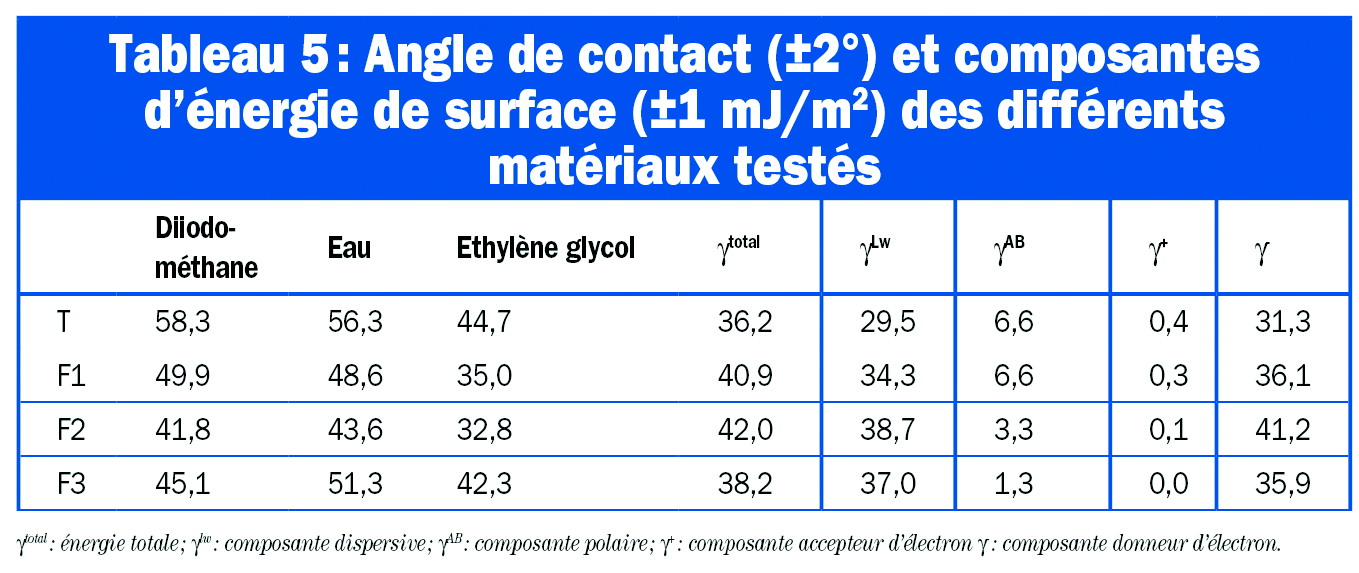
D’après ces résultats, comparés au témoin, on remarque que les trois formulations F1, F2 et F3 connaissent une augmentation de la composante apolaire γLw, cette augmentation est presque identique pour les trois formules. Par contre, concernant la composante polaire, on remarque que celle-ci a remarquablement chutée pour F3, elle est passée de 6,6 à 1,3 et aussi pour F2 elle est passée à 3,3.
.jpg)
Test d’adhésion
La figure 8 résume les résultats de dénombrements bactériens par unité de surface observée en MEB. Les valeurs constituent une moyenne de trois observations.
On remarque que l’adhésion décroît en intégrant l’huile de cade dans la formule du tube que ce soit pour P. aeruginosa ou E. coli en effet nous avons enregistré respectivement une réduction d’environ 71 % et 30 % pour F1, 60 % et 85 % pour F2 et 63 % et 41 % pour F3. Les figures 9 et 10 montrent des exemples de photos d’observation en microscopie électronique à balayage concernant E. coli et P. aeruginosa, où on voit clairement l’effet sur l’adhésion obtenu grâce aux nouvelles formules.
.jpg)
Discussion
La formation des biofilms passe par plusieurs étapes, d’abord l’attachement, la consolidation réalisée par la synthèse de composés extracellulaires et finalement la colonisation et la formation d’un biofilm mature. Dans cette étude on s’attache, pour lutter contre les biofilms, à agir en amont du processus entraînant leurs formations. L’attachement est l’étape qui précède la consolidation menant à la formation d’un biofilm mature. Cette étape peut être considérée comme étape-clé et décisive à la formation des biofilms. Cette phase est en général aspécifique et de courte durée (5 à 10 heures) [21]. Il est convenu que cette étape fait intervenir des interactions de nature physico-chimiques (interactions électrostatiques, électrodynamiques), et dépend de la nature du support et de son conditionnement préalable (présence de tubercules de corrosion, par exemple) [3, 21].
.jpg)
Du point de vue des observations microscopiques réalisées après le test d’adhésion, les résultats obtenus montrent tout d’abord que, d’une manière générale, l’adhésion initiale de P. aeruginosa est relativement plus importante qu’E. coli. Ces résultats concordent avec les travaux de plusieurs auteurs et ont été expliqués par la nature membranaire différentes entre les deux souches bactériennes et par le fait que plus les propriétés de la membrane de la souche sont hydrophobes, plus importante sera leur adhésion sur les surfaces solides [2, 21-23]. Boutaleb et al. 2007 [1] avaient souligné que l’adhésion de P. aeruosgina dépasse, en fonction du milieu, celle d’E. coli d’un facteur variable allant de 4 à 100 fois plus. Les mêmes souches, dans un milieu d’eau potable, étaient évaluées et P. aeruginosa se révélait plus hydrophobe.
Les nouvelles formules permettent une réduction de l’adhésion des souches. Cela concorde avec les résultats de plusieurs travaux qui ont évalué l’action de la présence de substances et extraits naturels sur la formation du biofilm. Lahaye et al. 2016 [24] ont montré l’évolution d’un biofilm à champignons filamenteux vers un biofilm bactérien positif après un traitement des canalisations par huiles essentielles, cette étude a été menée dans des fermes modèles d’élevage porcins.
Si l’on considère uniquement l’hydrophobicité, d’après les travaux antérieurs, il a été montré que l’adhésion aux substrats hydrophobes est plus importante comparée au support hydrophile [1]. Ceci est en désaccord avec les résultats de notre étude. En effet, les nouvelles formules présentent une hydrophobicité supérieure d’après l’angle de contact, et pourtant l’adhésion avait connue une diminution sur ces derniers. Ceci peut être expliqué par l’activité antibiotique générée par la nouvelle formulation (F1 et F2) intégrant les huiles : ail et cade. D’après la figure 8, Pseudomonas aeruginosa paraît être, contrairement à E. coli, plus sensible à l’huile de cade qu’à l’huile de l’ail. Ceci peut être confirmé au vu des photos de l’imagerie MEB : l’aspect des bactéries montre bien qu’à chaque fois que l’environnement est défavorable à la colonisation de la bactérie, celle-ci paraît avec une forme modifiée par rapport à la surface témoin et présente un slime secrété par elle-même pour se protéger. Bazargani et al. 2016 [25] avaient également montré que la présence d’une huile essentielle, cause des dommages morphologiques au niveau des cellules bactériennes, affecte la motilité des cellules, et modifie considérablement la structure du biofilm formé.
Pour F3, l’huile de ricin ne connaît pas d’activité antibiotique et pourtant, on remarque une diminution de l’adhésion des deux souches comparé au témoin. Il est à noter également que cette diminution est beaucoup plus marquée en présence de P. aeruginosa. Ceci est vraisemblablement attribuable à la modification des propriétés de la surface. En effet, selon les résultats du tableau 5, on remarque que pour cette surface, la composante polaire gAB avait considérablement diminuée. E. coli, est connu par son caractère acido-basique [1], le fait que la surface exprime moins ce caractère pourrait être à l’origine de la diminution de la colonisation. Pour P. aeruginosa, elle manifeste beaucoup plus son caractère basique et a plus de tendance pour les surfaces acides [1]. D’après les résultats, la composante accepteur d’électron avait chuté, ce qui peut éventuellement expliqué les observations.
Conclusion
Cette étude propose une nouvelle voie prometteuse de traitement préventif et moins dangereux pour lutter contre la formation des biofilms. Une nouvelle formulation du tube PVC destiné à l’adduction d’eau potable a été étudiée, elle constitue une substitution partielle de la fraction de lubrification dans la formule classique. Cette nouvelle formule présente bien l’effet souhaité. Les huiles naturelles sont connues pour leurs effets bénéfiques sur la santé, les résultats d’analyses structurales montrent leurs présences dans le tube fabriqué et montrent aussi que l’effet anti-biofilm n’est pas dû à des modifications des propriétés physico-chimiques de la surface, plutôt c’est l’effet d’expositions de sites biologiquement actifs.
Remerciements
Nous souhaitons exprimer nos remerciements à : M. Rachid Boutaam directeur général de la société EtuiPlast, Zone Industrielle de Bouskoura (Casablanca), Docteur Amane Jada de l’Institut des Sciences de Matériaux de Mulhouse - Centre National de Recherche Scientifiques et Technique (CNRST) du Maroc (Projet PPR2).

